猶素修飾在免疫調控中的作用及作為疾病治療潛在靶點的研究
在蛋白質修飾的神秘世界里,一種 2004 年被發現的新型類泛素化修飾 —— 猶素修飾(UFMylation),正逐漸揭開其在免疫調控中的關鍵作用。近日,廣東醫科大學基礎醫學院周軍智課題組在《Clinical and Translational Medicine》(中科院 1 區,IF=7.9)發表重磅綜述,系統梳理猶素系統如何通過精密調控免疫應答,成為連接細胞穩態與疾病發生的核心樞紐,為腫瘤、感染性疾病等的治療提供了全新靶點思路。
1. 先天免疫:抗病毒與炎癥反應的 “雙向開關”
在抗病毒防線中,猶素系統展現出 “雙刃劍” 效應:HSV-1 感染時,UFL1 與 STING 蛋白結合,抑制其泛素化降解,增強抗病毒信號;SenV 感染時,UFL1 聯合 14-3-3ε 蛋白促進 RIG-I 通路激活,加速干擾素產生。然而面對 EB 病毒,病毒蛋白 BILF1 卻劫持猶素系統,誘導 MAVS 蛋白猶素化并靶向溶酶體降解,實現免疫逃逸。在炎癥調控中,猶素系統抑制 LPS 或 IFN-γ 介導的巨噬細胞活化,減少 IL-6、TNF-α 等促炎因子釋放,避免過度免疫損傷。
2. 適應性免疫:腫瘤免疫與體液免疫的關鍵調控
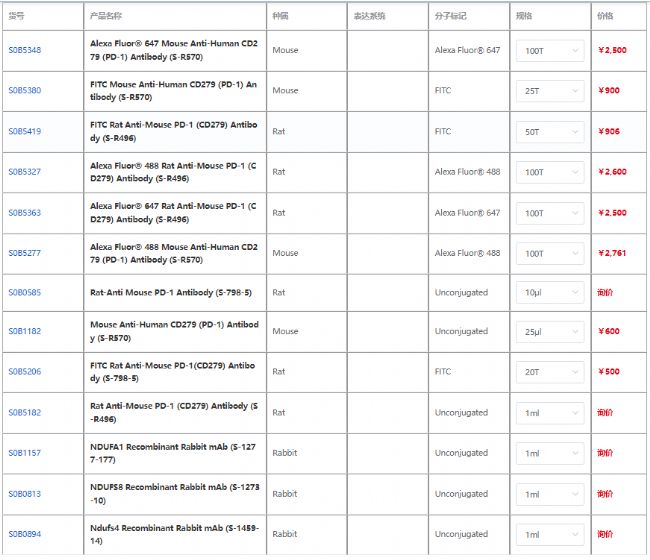
在腫瘤免疫領域,猶素系統通過 PD-1/PD-L1 通路發揮雙向調節:UFL1 促進 PD-L1 猶素化,加速其泛素化降解,增強抗腫瘤免疫;卻同時修飾 PD-1,抑制其降解并削弱 CD8+T 細胞活性。這種矛盾性為開發 “猶素修飾調節劑 + 免疫檢查點抑制劑” 聯合療法提供了理論依據,例如 UFSP2 抑制劑與 PD-1 抗體聯用可顯著抑制乳腺癌生長。針對體液免疫,銜接蛋白 UFBP1 通過抑制 PERK 通路,保障漿細胞發育及抗體分泌,其缺失將導致抗體產生障礙。
3. 跨系統對話:內分泌與免疫的隱秘聯系
猶素系統還扮演著內分泌 - 免疫交互的橋梁角色:調控腎上腺素受體的內質網運輸,維持應激反應平衡;增強雌激素受體穩定性,影響生殖相關免疫;在胰腺中高表達,保護胰島 β 細胞抵御內質網應激誘導的凋亡,揭示其在代謝性疾病中的潛在作用。
三、臨床轉化新方向:從機制解析到藥物靶點
該綜述首次全面整合猶素系統在免疫調控中的多維作用,尤其強調其在腫瘤免疫逃逸、病毒感染策略及自身免疫疾病中的關鍵節點功能。值得關注的是,猶素修飾酶(如 UFL1、UFSP2)的特異性干預,有望成為打破腫瘤免疫抑制微環境、增強抗病毒免疫應答的新突破口。周軍智團隊指出,針對猶素系統的小分子抑制劑(如 Compound 8)已進入臨床前研究,未來可探索其與現有療法的協同效應,為精準醫療開辟新賽道。
研究者背景:深耕蛋白修飾的前沿探索
通訊作者周軍智博士作為廣東醫科大學高層次人才,長期聚焦新型蛋白翻譯后修飾與腫瘤微環境研究。其團隊在國際頂級期刊發表多篇論文,揭示猶素修飾在腫瘤轉移、干細胞衰老等領域的調控機制,目前主持國家自然科學基金等多個項目,致力于解碼猶素系統的臨床應用潛力。
杭州斯達特 (www.starter-bio.com)志在為全球生命科學行業提供優質的抗體、蛋白、試劑盒等產品及研發服務。依托多個開發平臺:重組兔單抗、重組鼠單抗、快速鼠單抗、重組蛋白開發平臺(E.coli,CHO,HEK293,InsectCells),已正式通過歐盟98/79/EC認證、ISO9001認證、ISO13485。

一、猶素系統:從分子機制到生命調控網絡
作為真核生物中高度保守的修飾系統(除酵母等真菌),猶素系統由猶素分子(UFM1)、三級酶聯反應組件(E1 激活酶 UBA5、E2 結合酶 UFC1、E3 連接酶 UFL1)、去修飾酶(UFSP1/2)及銜接蛋白(DDRGK1、C53)構成。其核心功能在于通過可逆的賴氨酸修飾,精準調控靶蛋白功能:成熟 UFM1 經 UBA5/UFC1/UFL1 催化共價結合底物,完成使命后由 UFSP1/2 去除,形成動態平衡。這一過程深度參與內質網穩態、基因組穩定性、細胞周期等基礎生命活動,其失調與髖關節發育不良、嬰兒腦病、小頭畸形等神經發育疾病密切相關。
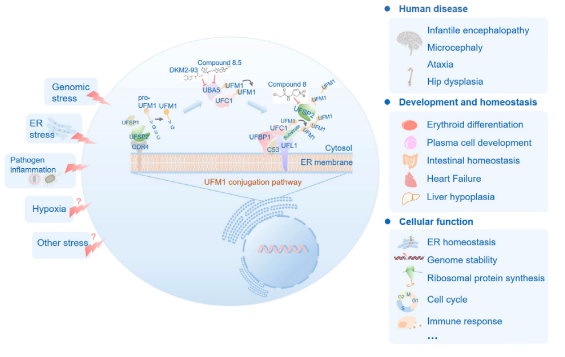
猶素化組成和功能
1. 先天免疫:抗病毒與炎癥反應的 “雙向開關”
在抗病毒防線中,猶素系統展現出 “雙刃劍” 效應:HSV-1 感染時,UFL1 與 STING 蛋白結合,抑制其泛素化降解,增強抗病毒信號;SenV 感染時,UFL1 聯合 14-3-3ε 蛋白促進 RIG-I 通路激活,加速干擾素產生。然而面對 EB 病毒,病毒蛋白 BILF1 卻劫持猶素系統,誘導 MAVS 蛋白猶素化并靶向溶酶體降解,實現免疫逃逸。在炎癥調控中,猶素系統抑制 LPS 或 IFN-γ 介導的巨噬細胞活化,減少 IL-6、TNF-α 等促炎因子釋放,避免過度免疫損傷。
2. 適應性免疫:腫瘤免疫與體液免疫的關鍵調控
在腫瘤免疫領域,猶素系統通過 PD-1/PD-L1 通路發揮雙向調節:UFL1 促進 PD-L1 猶素化,加速其泛素化降解,增強抗腫瘤免疫;卻同時修飾 PD-1,抑制其降解并削弱 CD8+T 細胞活性。這種矛盾性為開發 “猶素修飾調節劑 + 免疫檢查點抑制劑” 聯合療法提供了理論依據,例如 UFSP2 抑制劑與 PD-1 抗體聯用可顯著抑制乳腺癌生長。針對體液免疫,銜接蛋白 UFBP1 通過抑制 PERK 通路,保障漿細胞發育及抗體分泌,其缺失將導致抗體產生障礙。
3. 跨系統對話:內分泌與免疫的隱秘聯系
猶素系統還扮演著內分泌 - 免疫交互的橋梁角色:調控腎上腺素受體的內質網運輸,維持應激反應平衡;增強雌激素受體穩定性,影響生殖相關免疫;在胰腺中高表達,保護胰島 β 細胞抵御內質網應激誘導的凋亡,揭示其在代謝性疾病中的潛在作用。
三、臨床轉化新方向:從機制解析到藥物靶點
該綜述首次全面整合猶素系統在免疫調控中的多維作用,尤其強調其在腫瘤免疫逃逸、病毒感染策略及自身免疫疾病中的關鍵節點功能。值得關注的是,猶素修飾酶(如 UFL1、UFSP2)的特異性干預,有望成為打破腫瘤免疫抑制微環境、增強抗病毒免疫應答的新突破口。周軍智團隊指出,針對猶素系統的小分子抑制劑(如 Compound 8)已進入臨床前研究,未來可探索其與現有療法的協同效應,為精準醫療開辟新賽道。
研究者背景:深耕蛋白修飾的前沿探索
通訊作者周軍智博士作為廣東醫科大學高層次人才,長期聚焦新型蛋白翻譯后修飾與腫瘤微環境研究。其團隊在國際頂級期刊發表多篇論文,揭示猶素修飾在腫瘤轉移、干細胞衰老等領域的調控機制,目前主持國家自然科學基金等多個項目,致力于解碼猶素系統的臨床應用潛力。
從基礎分子機制到復雜疾病網絡,猶素系統的免疫調控密碼正逐步破譯。這一新興領域不僅改寫了我們對蛋白質修飾與免疫交互的認知,更預示著以猶素修飾為靶點的精準治療時代即將到來。隨著基礎研究與轉化醫學的深度融合,這一 “免疫新樞紐” 有望成為未來疾病治療的關鍵鑰匙。
產品信息
杭州斯達特 (www.starter-bio.com)志在為全球生命科學行業提供優質的抗體、蛋白、試劑盒等產品及研發服務。依托多個開發平臺:重組兔單抗、重組鼠單抗、快速鼠單抗、重組蛋白開發平臺(E.coli,CHO,HEK293,InsectCells),已正式通過歐盟98/79/EC認證、ISO9001認證、ISO13485。
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com