文獻解讀:新型探針解析胞內(nèi)腺苷的在體時空動態(tài)及調(diào)控機制

2025年5月7日,北京大學藥學院王晶課題組聯(lián)合中國科學院遺傳與發(fā)育生物學研究所武照伐課題組和北京大學生命科學學院李毓龍課題組,在Nature Communications雜志發(fā)表題為“A high-performance fluorescent sensor spatiotemporally reveals cell-type specific regulation of intracellular adenosine in vivo”的文章,該研究成功開發(fā)了首個用于活體檢測胞內(nèi)腺苷的基因編碼熒光探針HypnoS(Hypersensitive intracellular adenosine Sensor),并借助活體成像與光遺傳技術(shù)等手段,探究了活體動物中胞內(nèi)腺苷時空動態(tài)上的細胞特異性調(diào)控,以及背后的分子調(diào)控機制(圖1)。
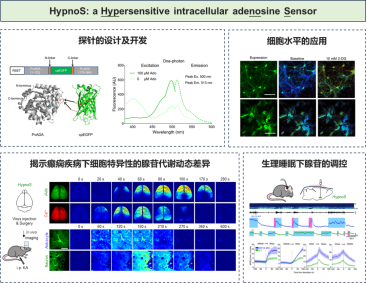
圖1. HypnoS的設(shè)計、驗證及應(yīng)用總結(jié)
研究團隊基于循環(huán)重排綠色熒光蛋白(cpEGFP)與腺苷脫氨酶(PvADA),在篩選了超過3000個突變體后,成功構(gòu)建了新型熒光探針HypnoS(取名古希臘神話中的“睡神”)。HypnoS具備極高的靈敏度(響應(yīng)幅度>900%)、適宜的親和力(EC50 ~11 μM)、亞秒級動力學特性及良好的選擇性(圖2),重要的是HypnoS表達對神經(jīng)元的正常生理過程無明顯影響,這些特性使其成為檢測生理和病理條件下胞內(nèi)腺苷變化的理想工具。

圖2. HypnoS探針的開發(fā)和體外刻畫。a. 探針的構(gòu)成;b. 探針單光子光譜性質(zhì);c. 探針親和力,其中HypnoS-mut是探針對照;d. 亞秒級別的動力學特性;e. 優(yōu)異的特異性;f. 探針幾乎不具備酶活性。
在細胞水平上,腦中不同的類型細胞對胞內(nèi)腺苷(iAdo)生成、代謝及釋放的差異仍不明確,胞外腺苷(eAdo)來源于神經(jīng)元還是相鄰的膠質(zhì)細胞在領(lǐng)域內(nèi)存在爭議。利用新型HypnoS的可遺傳編碼特性,作者將HypnoS探針分辨表達在了神經(jīng)元及星形膠質(zhì)細胞,在原代培養(yǎng)的細胞、急性腦片以及自由活動小鼠等多種體系中實現(xiàn)了對iAdo動態(tài)的細胞特異性監(jiān)測。研究發(fā)現(xiàn)神經(jīng)元和星形膠質(zhì)細胞腺苷的水平、動力學及釋放存在顯著差異(圖3),提示兩種細胞類型對腺苷穩(wěn)態(tài)的不同貢獻。
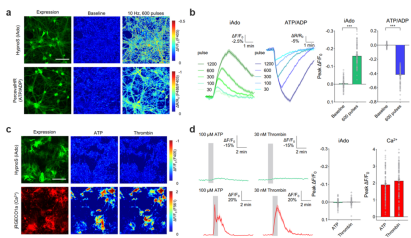
圖3. 檢測原代培養(yǎng)的神經(jīng)元與星形膠質(zhì)細胞中腺苷及ATP代謝差異。a和b. 神經(jīng)元活動過程中腺苷代謝和ATP能量代謝之間的關(guān)系;c和d. 星形膠質(zhì)細胞鈣活動時胞內(nèi)腺苷的動態(tài)變化。
在病理過程中(如癲癇),腺苷被認為是重要的內(nèi)源性抗驚厥因子。利用新型HypnoS探針結(jié)合在體大視場成像,作者首次在活體小鼠整個大腦皮層尺度可視化了急性癲癇發(fā)作期間iAdo的動態(tài)變化。研究發(fā)現(xiàn)iAdo變化顯著滯后于癲癇引發(fā)的神經(jīng)元鈣活動并持續(xù)更長時間,這與iAdo在癲癇發(fā)作后的潛在神經(jīng)保護作用一致(圖4)。進一步地,作者運用活體雙光子成像技術(shù),在單細胞水平解析了iAdo在神經(jīng)元及星形膠質(zhì)細胞中的動態(tài)變化,并發(fā)現(xiàn)星形膠質(zhì)細胞能夠以更快的速度降解iAdo(圖4),這一發(fā)現(xiàn)拓展了不同細胞對癲癇期間腺苷代謝調(diào)控機制的理解。
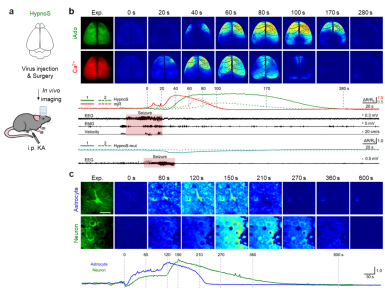
圖4. 利用HypnoS檢測癲癇發(fā)作過程中胞內(nèi)腺苷的動態(tài)變化。a. 示意圖;b. 結(jié)合大視場成像檢測小鼠癲癇發(fā)作過程HypnoS與鈣信號之間的時空關(guān)系;c. 結(jié)合在體雙光子檢測小鼠癲癇發(fā)作過程中神經(jīng)元與星形膠質(zhì)細胞胞內(nèi)腺苷動態(tài)差異。
在生理過程中(如睡眠-覺醒),腺苷被認為是調(diào)控睡眠穩(wěn)態(tài)的重要分子。研究團隊利用HypnoS探針結(jié)合光纖和腦電、肌電記錄,在小鼠基底前腦研究中捕捉到清醒與REM睡眠時期胞內(nèi)腺苷升高,NREM睡眠時期下降的現(xiàn)象。研究表明,ENT1/2在神經(jīng)元中主導腺苷釋放,而在星形膠質(zhì)細胞中促進腺苷攝取,揭示了兩種細胞在睡眠穩(wěn)態(tài)中的分工機制(圖5),這一發(fā)現(xiàn)為通過調(diào)控腺苷水平干預睡眠障礙提供了分子基礎(chǔ)。
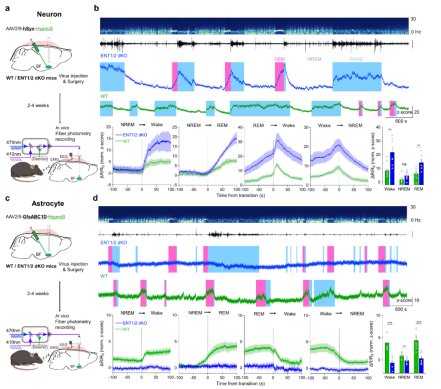
圖5. 睡眠-覺醒周期中胞內(nèi)腺苷的動態(tài)及細胞特異性調(diào)控。a和b. 睡眠-覺醒周期中ENT1/2 介導的腺苷轉(zhuǎn)運在神經(jīng)元中的作用。c和d. 睡眠-覺醒周期中ENT1/2 介導的腺苷轉(zhuǎn)運在星形膠質(zhì)細胞中的作用。
參考文獻:Wei, Q., Bai, Z., Wang, L. et al. A high-performance fluorescent sensor spatiotemporally reveals cell-type specific regulation of intracellular adenosine in vivo. Nat Commun 16, 4245 (2025). https://doi.org/10.1038/s41467-025-59530-7
創(chuàng)作聲明:本文是在原英文文獻基礎(chǔ)上進行解讀,存在觀點偏向性,僅作分享,請參考原文深入學習。


想了解更多內(nèi)容,獲取相關(guān)咨詢請聯(lián)系
電 話:+86-0731-84428665
伍經(jīng)理:+86-180 7516 6076
徐經(jīng)理:+86-138 1744 2250
郵 箱:consentcs@163.com