調控多種生物功能的肌動蛋白波在多細胞范圍內的生物學作用
30年前,研究人員在土壤變形蟲盤狀變形蟲中首次觀察到,細胞皮層中的肌動蛋白結構可以形成動態的波浪狀圖案1,2。隨后,越來越多的其他類型的細胞中也發現了肌動蛋白波,包括中性粒細胞、樹突狀細胞、T 細胞、神經元、內皮細胞、成纖維細胞和角膜細胞1,3,4。
雖然肌動蛋白波在形態、傳播速度和生化成分上存在很大差異3(圖1),但它們可以被廣泛地定義為“在肌動蛋白皮層中以波狀方式傳播的絲狀肌動蛋白密度增加的微米級細胞骨架區域”1。早期的許多研究工作都在探討肌動蛋白在細胞遷移和分裂中的作用1,但現在人們發現了肌動蛋白更廣泛的功能作用。本文我們將回顧自最初發現肌動蛋白波以來,我們對肌動蛋白波的認識是如何發展的,并重點介紹近期的重要發現,這些發現表明肌動蛋白波在多細胞范圍內發揮著重要的生物學作用。
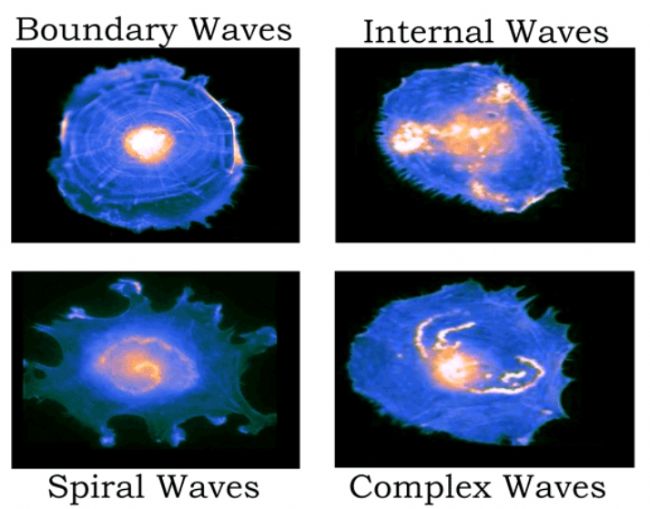
圖1:在培養的人主動脈內皮細胞中觀察到的不同肌動蛋白波型的示意圖(Riedl M. et al Nat Commun. 2023; ref. 4)
1.肌動蛋白波的自發產生
早期的一個關鍵問題涉及肌動蛋白波的起源,通過應用其它波動現象的理論原理,證明了細胞肌動蛋白皮層具有可激發介質的特性5-7。這些系統能夠自發產生波,就細胞皮層而言,系統的調節(即激活閾值)取決于肌動蛋白核聚體的時空分布和F-肌動蛋白組裝速率之間的平衡。當局部核聚體濃度超過一定閾值時,就會產生肌動蛋白波8。F-肌動蛋白和肌動蛋白核聚體之間的負反饋完成了典型的應激系統的激活-抑制動力學7,9。因此,產生和傳播肌動蛋白波的能力是肌動蛋白皮層作為“主動適應材料”的固有特征10。
2.肌動蛋白波引導細胞運動
在自適應可激發介質中,外部擾動可以引起波的形成。早期的一個重要發現是纖毛膜中由壓力誘導的后向肌動蛋白波,這種波將α-肌動蛋白和MYLK信號復合物從纖毛膜頂端輸送到基部,以控制收縮/伸展周期11。還有研究表明,波形調節復合體在中性粒細胞HL-60中產生的肌動蛋白波,實驗觀察與理論研究中發展的自激活和延遲抑制(由于F-肌動蛋白的緩慢擴散)模型一致12,作者認為細胞趨化運動依賴于多個肌動蛋白波的共同作用。
有研究者提出,自發的肌動蛋白波動力學可以解釋阿米巴樣細胞的隨機行走6,7,這一點在樹突狀細胞中得到了很好的證明9。樹突狀細胞在巡視組織尋找病原體時表現出隨機行走行為,將它的運動軌跡繪制出來,并可根據其固有的肌動蛋白波動力學建模,說明了這些細胞如何通過調節肌動蛋白核聚體的分布和肌動蛋白聚合速率來自適應地控制其遷移模式。眾所周知,Arp2/3復合體和Ena/VASP肌動蛋白核聚體對樹突狀細胞的正常運動非常重要9,13。
3.調節肌動蛋白動力學的其他應激網絡
對肌動蛋白波的研究也揭示了相關信號分子的脈沖行為,這些分子表現出應激的動力學10,14。例如,在卵母細胞和胚胎細胞中進行細胞分裂時,Rho 活性波在肌動蛋白波之前傳播15。小GTP酶(如RhoA)由于其活性的自催化傳播,可以充當應激的快速擴散激活劑16。與肌動蛋白波類似,延遲來自 F-肌動蛋白介導的對波后對 Rho 活性抑制的負反饋,從而導致觀察到波動模式15。因此,應激的激活-抑制特性對Rho活性影響也是明顯的。
在線蟲胚胎中可以觀察到一種相關的機制,其中延遲的負反饋來自兩個Rho GAP(RGA-3/4),它們被F-肌動蛋白招募以消除前導Rho波后的小GTP酶活性10,17。其他研究結果表明,Ras活性進一步微調了肌動蛋白波的動力學,相對較小的變化就足以引起波的大小、速度和射速的巨大變化18。
綜上所述,研究人員提出了一個新概念——獨特的信號轉導應激網絡(STEN),它可以感知化學信息,與細胞骨架應激網絡(CEN)對物理線索的感知類似,CEN完全依賴于肌球蛋白皮層作為應激的固有屬性14。在接觸類膠原納米脊的細胞中,STEN和CEN衍生的波被限制在不同的區域,CEN波更有可能直接沿著脊線發起19。因此,STEN和CEN應激系統之間的串擾被認為是整合不同環境信號以正確引導細胞遷移的關鍵。
4.肌動蛋白波的新功能
為了支持上述觀點,已證實 CEN 和 STEN 系統都能感知電場。值得注意的是,皮膚傷口會迅速激發強大的生物電場,在傷口修復過程中提供重要的細胞引導信號20,并隨著傷口的愈合過程而逐漸減弱21。細胞在電場中的定向遷移是再生和發育以及傷口愈合中的一個重要現象22。
在盤狀芽孢桿菌細胞中,可以看到電場極化肌動蛋白波核并引導波的傳播,從而介導趨電性22。雖然這些電場在全局范圍內引導肌動蛋白波,但即使改變場的方向,納米脊仍能誘導局部的肌動蛋白波(通過 CEN 系統)跟隨脊,這意味著可應激系統的局部和全局調節都以互補的方式發揮作用,可以通過肌動蛋白動力學的變化來解釋多個指導信號的轉導23。
實際上,肌動蛋白絲作為“生物電線”的特性早在30年前就已被發現了24,而且已經證實肌動蛋白絲會根據電場定向排列25。由于內源性生物電網絡正逐漸成為細胞發育和再生過程中模式控制的一個自主層26,生物電引導的肌動蛋白波似乎有可能在形態發生(包括傷口修復)過程中作為細胞組織的基礎,以響應支配生物模式形成的電信號。
另一方面,眾所周知,即使在常氧條件下,癌細胞也會上調糖酵解(稱為沃伯格效應)。新的研究結果顯示,糖酵解酶被募集到細胞皮層,并與肌動蛋白波共定位27,這表明癌細胞可以利用糖酵解快速產生局部 ATP,從而皮層產生的直接能量驅動遷移28。雖然之前的研究已將糖酵解作為癌細胞運動的一種能量來源29,30,但糖酵解與肌動蛋白波的功能性關聯為沃伯格效應提供了新的機理認識。與未轉化的細胞相比,癌細胞表現出更高的糖酵解和肌動蛋白波活性,并且隨著轉移指數的增加而逐漸增強27。
5.新的發展和展望
在最近的一項研究中,發現了細胞群中肌動蛋白波的同步性和集體運動4。與在其他細胞類型中觀察到的一致,人主動脈內皮細胞中肌動蛋白波的成核頻率與遷移速度相關,但與離體的細胞在低密度下的運動方式不同。在細胞匯合時,可觀察到連貫的集體運動,這可能與肌動蛋白波的成核頻率同步有關。作者將此稱為“頻率鎖定”,以實現有序的集體運動,推導出相關的耦合機制將是未來研究的一個引人入勝的方向。
參考文獻:
【1】Beta C, Edelstein-Keshet L, Gov N, Yochelis A. From actin waves to mechanism and back: How theory aids biological understanding. Elife. 2023;12:e87181. https://doi.org/10.7554/eLife.87181.
【2】Vicker MG, Xiang W, Plath PJ, Wosniok W. Pseudopodium extension and amoeboid locomotion in Dictyostelium discoideum: Possible autowave behaviour of F-actin. Physica D. 1997;101(3–4):317–332. https://doi.org/10.1016/S0167-2789(96)00224-2.
【3】Beta C, Gov NS, Yochelis A. Why a large-scale mode can be essential for understanding intracellular actin waves. Cells. 2020;9(6):1533. https://doi.org/10.3390/cells9061533.
【4】Riedl M, Mayer I, Merrin J, Sixt M, Hof B. Synchronization in collectively moving inanimate and living active matter. Nat Commun. 2023;14(1):5633. https://doi.org/10.1038/s41467-023-41432-1.
【5】Doubrovinski K, Kruse K. Cytoskeletal waves in the absence of molecular motors. Europhys Lett. 2008;83(1):18003. https://doi.org/10.1209/0295-5075/83/18003.
【6】Doubrovinski K, Kruse K. Cell motility resulting from spontaneous polymerization waves. Phys Rev Lett. 2011;107(25):258103. https://doi.org/10.1103/PhysRevLett.107.258103.
【7】Ecker N, Kruse K. Excitable actin dynamics and amoeboid cell migration. PLoS One. 2021;16(2):e0246311. https://doi.org/10.1371/journal.pone.0246311.
【8】Motoike IN, Adamatzky A. Three-valued logic gates in reaction–diffusion excitable media. Chaos Solitons Fractals. 2005;24(1):107–114. https://doi.org/10.1016/j.chaos.2004.07.021.
【9】Stankevicins L, Ecker N, Terriac E, et al. Deterministic actin waves as generators of cell polarization cues. Proc Natl Acad Sci U S A. 2020;117(2):826–835. https://doi.org/10.1073/pnas.1907845117.
【10】Staddon MF, Munro EM, Banerjee S. Pulsatile contractions and pattern formation in excitable actomyosin cortex. PLoS Comput Biol. 2022;18(3):e1009981. https://doi.org/10.1371/journal.pcbi.1009981.
【11】Giannone G, Dubin-Thaler BJ, Döbereiner H-G, Kieffer N, Bresnick AR, Sheetz MP. Periodic lamellipodial contractions correlate with rearward actin waves. Cell. 2004;116(3):431–443. https://doi.org/10.1016/s0092-8674(04)00058-3.
【12】Weiner OD, Marganski WA, Wu LF, Altschuler SJ, Kirschner MW. An actin-based wave generator organizes cell motility. PLoS Biol. 2007;5(9):e221. https://doi.org/10.1371/journal.pbio.0050221.
【13】Visweshwaran SP, Nayab H, Hoffmann L, Gil M, Liu F, Kühne R, Maritzen T. Ena/VASP proteins at the crossroads of actin nucleation pathways in dendritic cell migration. Front Cell Dev Biol. 2022;10:1008898. https://doi.org/10.3389/fcell.2022.1008898
【14】Miao Y, Bhattacharya S, Banerjee T, et al. Wave patterns organize cellular protrusions and control cortical dynamics. Mol Syst Biol. 2019;15(3):e8585. https://doi.org/10.15252/msb.20188585.
【15】Bement WM, Leda M, Moe AM, et al. Activator–inhibitor coupling between Rho signalling and actin assembly makes the cell cortex an excitable medium. Nat Cell Biol. 2015;17(11):1471–1483. https://doi.org/10.1038/ncb3251.
【16】Tsyganov MA, Kolch W, Kholodenko BN. The topology design principles that determine the spatiotemporal dynamics of G-protein cascades. Mol Biosyst. 2012;8(3):730–743. https://doi.org/10.1039/c2mb05375f.
【17】Michaux JB, Robin FB, McFadden WM, Munro EM. Excitable RhoA dynamics drive pulsed contractions in the early C. elegans embryo. J Cell Biol. 2018;217(12):4230–4252. https://doi.org/10.1083/jcb.201806161.
【18】Lin Y, Pal DS, Banerjee P, et al. Ras-mediated homeostatic control of front–back signaling dictates cell polarity. bioRxiv. Preprint posted online September 1, 2023. https://doi.org/10.1101/2023.08.30.555648.
【19】Yang Q, Miao Y, Banerjee P, et al. Nanotopography modulates intracellular excitable systems through cytoskeleton actuation. Proc Natl Acad Sci U S A. 2023;120(19):e2218906120. https://doi.org/10.1073/pnas.2218906120.
【20】Tai G, Tai M, Zhao M. Electrically stimulated cell migration and its contribution to wound healing. Burns Trauma. 2018;6:20. https://doi.org/10.1186/s41038-018-0123-2
【21】Nuccitelli R, Nuccitelli P, Ramlatchan S, Sanger R, Smith PJS. Imaging the electric field associated with mouse and human skin wounds. Wound Repair Regen. 2008;16(3):432–441. https://doi.org/10.1111/j.1524-475x.2008.00389.x.
【22】Yang Q, Miao Y, Campanello LJ, et al. Cortical waves mediate the cellular response to electric fields. Elife. 2022;11:e73198. https://doi.org/10.7554/eLife.73198.
【23】Bull AL, Campanello L, Hourwitz MJ, Yang Q, Zhao M, Fourkas JT, Losert W. Actin dynamics as a multiscale integrator of cellular guidance cues. Front Cell Dev Biol. 2022;10:873567. https://doi.org/10.3389/fcell.2022.873567.
【24】Lin EC, Cantiello HF. A novel method to study the electrodynamic behavior of actin filaments. Evidence for cable-like properties of actin. Biophys J. 1993;65(4):1371–1378. https://doi.org/10.1016/S0006-3495(93)81188-3.
【25】Arsenault ME, Zhao H, Purohit PK, Goldman YE, Bau HH. Confinement and manipulation of actin filaments by electric fields. Biophys J. 2007;93(8):L42–L44. https://doi.org/10.1529/biophysj.107.114538.
【26】Levin M. Endogenous bioelectrical networks store non-genetic patterning information during development and regeneration. J Physiol. 2014;592(11):2295–2305. https://doi.org/10.1113/jphysiol.2014.271940.
【27】Zhan HD, Borleis J, Janetopoulos C, Devreotes P. Abstract 288: Glycolysis is enriched to propagating waves in cell cortex as a new mechanism for cancer progression. Cancer Res. 2023;83(7_Suppl):288. https://doi.org/10.1158/1538-7445.am2023-288.
【28】Zheng J. Energy metabolism of cancer: Glycolysis versus oxidative phosphorylation. Oncol Lett. 2012;4(6):1151–1157. https://doi.org/10.3892/ol.2012.928.
【29】Shiraishi T, Verdone JE, Huang J, et al. Glycolysis is the primary bioenergetic pathway for cell motility and cytoskeletal remodeling in human prostate and breast cancer cells. Oncotarget. 2015;6(1):130–143. https://doi.org/10.18632/oncotarget.2766.
【30】Zanotelli MR, Zhang J, Reinhart-King CA. Mechanoresponsive metabolism in cancer cell migration and metastasis. Cell Metab. 2021;33(7):1307–1321. https://doi.org/10.1016/j.cmet.2021.04.002.