研究循環應變下NSCs分化:星形膠質細胞對神經元機械保護機制
神經干細胞(NSC)是中樞神經系統中所有神經元和神經膠質細胞的來源。NSCs 感知位于其特殊細胞外環境(稱為神經干細胞生態位)中的化學和機械線索。在這種特殊的微環境中,NSCs 和祖細胞由許多調節干細胞特性的細胞外信號提供。
由于血液脈動,腦組織持續運動,組織變形幅度接近高達 30%。因此,雖然經常被忽視,但無處不在的機械線索會影響生態位,例如周圍微環境的剛度或或由于微環境的復雜結構及其相互連接的細胞外蛋白質網絡而產生的管狀結構網絡。Arumoli 及其同事曾報告了應變作為影響 NSCs 的機械線索。此外,脈動血管施加的機械應變可能會對 NSCs 產生實質性的影響。研究表明,機械因素本質上影響分化模式和細胞系定型。然而,關于循環應變作為 NSCs 命運線索的作用知之甚少。
德國 Juelich 研究中心及科隆大學醫學院研究團隊之前的實驗表明,這種脈動運動可以通過在可拉伸彈性體上培養的細胞來在體外進行模擬。使用該系統,循環拉伸的神經元在垂直于單軸應變的方向上生長。這種細胞重新定向是大多數哺乳動物細胞在拉伸時的特征反應。值得注意的是,循環拉伸誘導神經元分支的生長,表明機械應變參與了其發育過程。在后期的一項研究中,該團隊進一步探討了循環單軸應變對原代大鼠 NSCs 及其后代的影響。相關研究成果發表在 Frontiers in Cellular Neuroscience 期刊題為“NSCs Under Strain—Unraveling the Mechanoprotective Role of Differentiating Astrocytes in a Cyclically Stretched Coculture With Differentiating Neurons”。

由于遷移細胞(如NSCs)的高細胞動力學,研究人員懷疑循環底物應變會在多大程度上使生長在彈性體頂部的 NSCs 變形,利用自制的基于交聯聚二甲基硅氧烷(PDMS)彈性體拉伸系統,腔室以 15% 的振幅和 300 mHz 的頻率單軸拉伸(這種拉伸方案已被證明可以誘導皮質神經元的明確機械反應)。首先檢測對循環應變的即時反應,通過活細胞顯微鏡觀察 NSCs 的機械變形。振幅逐步增加 4%,直到應變的 28%,并在釋放位置再次成像(圖1 A)。底物應變使神經元胞體細胞和 NSCs 的突起均發生變形,而且沿著拉伸方向排列的細胞過程跟隨底物拉伸(圖1 B),而垂直于拉伸方向的細胞過程沒有發生明顯的伸長。在施加28%的底物應變后,NSCs 顯示細胞體拉伸 25.5%(圖1 C)。NSCs 不會受到底物變形的負面影響,因為根據碘化丙啶評估它們不會收縮并且保持活力(圖1 D、E)。
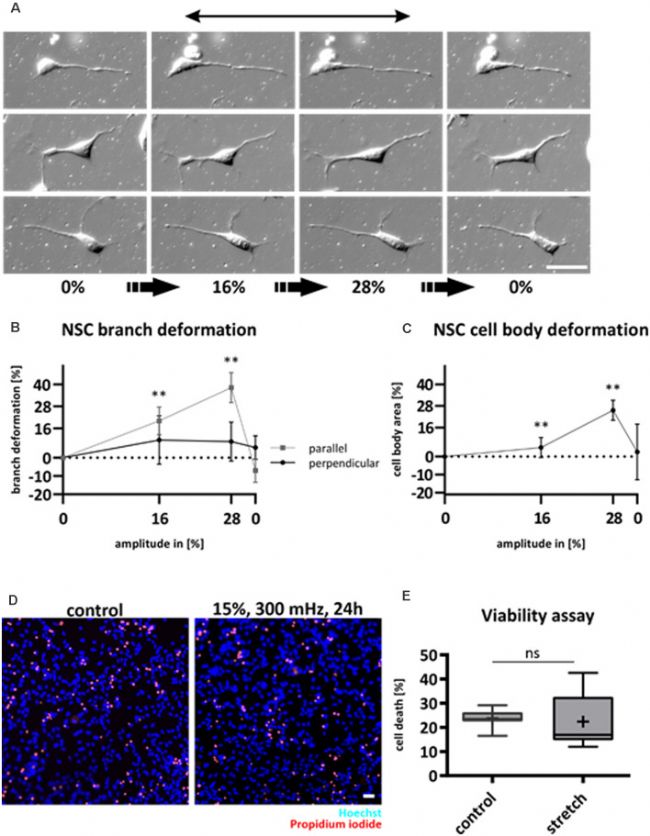
圖1 NSCs遵循底物變形,不受循環應變的影響。
接下來,研究了循環機械應變對 NSCs 特征功能的影響,即增殖,分化和譜系決定(lineage commitment)。與未拉伸對照相比,在有絲分裂原 FGF 存在下循環拉伸24小時顯著降低了 NSC 的增殖率。然而,有絲分裂原停用后5天開始分化的譜系決定并沒有被整個時間內應用的循環機械拉伸所改變。此外,用干性標記物 Sox2 染色證明,有絲分裂原停用5天后的循環拉伸不影響仍未分化的 NSCs 的百分比,這表明這種機械刺激既不影響 NSC 分化的速度,也不影響 NSC 分化的命運。
雖然大多數哺乳動物細胞大致垂直于單軸循環應變排列以減少其機械應力,但在這里首次發現 NSCs 平行于拉伸方向排列(圖2 A-C)。NSCs 的細胞骨架絲在細胞內具有不同的空間分布,導致其對應變有明顯的重定向模式(圖2 B)。然而,肌動蛋白更多地定位于外周部分和細胞突起,只有適度的重新排列。有趣的是,實驗沒有觀察到任何應力纖維的形成,肌動蛋白細胞骨架分布在拉伸組和對照組中相似。總的來說,細胞骨架標記在暴露于循環拉伸24小時后顯示出平行于應變的重新定向(圖2 C)。通過半定量分析,發現拉伸 NSC 中微管蛋白和巢蛋白染色的圖像強度增加,這表明拉伸誘導了兩個細胞骨架系統的細胞骨架增強(圖2 D)。
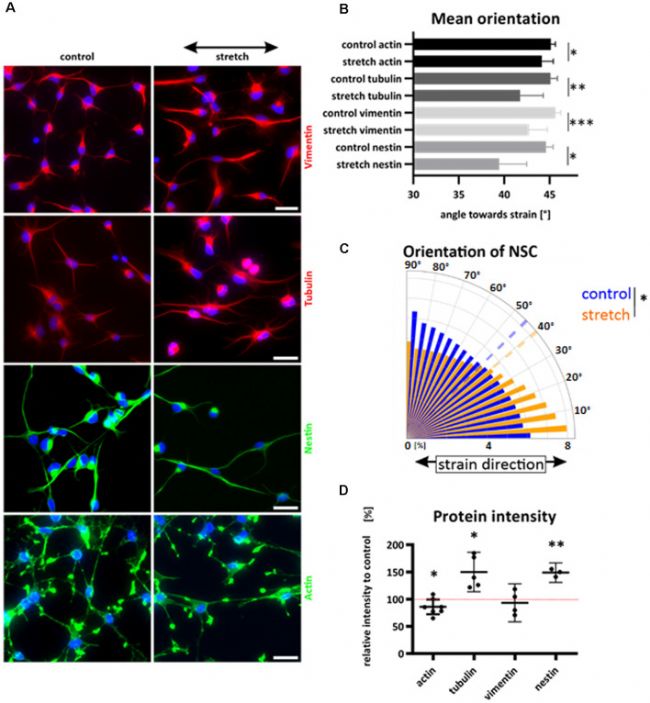
圖2 神經干細胞在應變和細胞骨架重分布下的重定向。
由于 NSCs 在拉伸方向上重新定向,因此接著研究了 NSCs 在分裂原退出誘導的分化過程中如何對應變作出反應。與未分化的 NSC 類似,NSC 衍生的年輕星形膠質細胞平行于循環應變排列。在分化過程中拉伸的星形膠質細胞與未拉伸的對照細胞相比,GFAP(膠質纖維酸性蛋白)排列明顯向應變方向轉移。相比之下,NSC 衍生的年輕神經元沒有顯示出任何重新定向。
為了研究這種重新定向行為是否是星形膠質細胞分化的一個主動的、持續的過程,在拉伸3天后將單軸應變的方向旋轉90°,這是一個已經可以看到定向生長的時間點。旋轉人為地迫使星形膠質細胞向遠離拉伸的方向運動。然而,持續2天的循環拉伸恢復了星形膠質細胞的平行方向,強調了應變方向的排列特征是年輕星形膠質細胞對循環應變的穩定和積極的機械反應。這表明,神經干細胞分化過程中的循環應變在神經表型缺乏機械反應的情況下使星形膠質細胞向拉伸方向重新定向。
細胞與應變的平行排列先前被描述為依賴于 GTPase RhoA 的激活,并且與內皮細胞和骨肉瘤細胞中缺乏應力纖維有關。由于觀察到 NSCs 中缺乏中心應力纖維,因此假設 NSCs 中缺乏收縮性可能是導致這些細胞在最大機械負荷方向排列的原因。為了驗證這一假設,通過溶血磷脂酸(LPA)激活 RhoA 來增加 NSCs 的收縮性,并觀察到 NSCs 中中心應力纖維的清晰形成與應變無關。此外,在拉伸應用后,應力纖維誘導顯著降低了 NSCs 在最大機械負荷方向的定向行為,從而降低了之前發現的 NSCs 的機械響應。
相反,應力纖維存在于產后星形膠質細胞中。與未拉伸的細胞相比,拉伸后在垂直方向上可以檢測到輕微的重新定向,值得注意的是,星形膠質細胞的 GFAP 細胞骨架不受循環拉伸的影響。在24小時的拉伸后,它沒有顯示出任何定向方向,導致出生后星形膠質細胞隨機分布的長細胞形狀。
為了進一步闡明星形膠質細胞和神經元之間以及分化階段觀察到的差異,最后,進一步評估了星形膠質細胞/神經元共培養中不同細胞比例對循環應變的反應(圖3 A、B)。雖然分離的神經元與應變垂直排列(圖3 B、C),但共培養中神經元的重新排列取決于星形膠質細胞的比例(圖3 B)。隨著星形膠質細胞數量的增加,在相同數量的星形膠質細胞時(1:1),神經元的排列不斷減少,導致神經元細胞的隨機定向。然而,當共培養的星形膠質細胞較少時(4:1),神經元細胞保持其機械反應,相對于應變保持垂直方向排列。共聚焦顯微鏡和3D重建顯示,混合培養中皮層神經元在產后星形膠質細胞上生長(圖3 D)。這些數據不僅證實了之前顯示的星形膠質細胞和神經元分化的協同細胞生長,而且還證明了星形膠質細胞對分化的神經元具有機械保護功能。
實驗在 LPA 存在下的神經元拉伸實驗以及神經元和星形膠質細胞的共培養中進一步分析了這一假設。這些數據證實了純神經元相對于拉伸在垂直方向上的重新定向。有趣的是,即使 RhoA 被激活,星形膠質細胞以1-1的比例存在也保留了它們對神經元的機械保護作用。如果 RhoA 在整個24小時的拉伸時間內或僅在拉伸的最后40分鐘被激活,這種效果保持穩定。
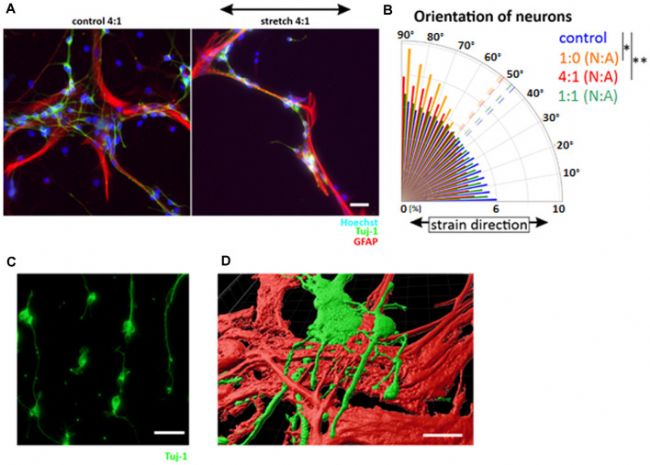
圖3 產后星形膠質細胞的機械保護作用。
總之,這些發現可能突出了星形膠質細胞在清除對神經元表型的機械影響方面的重要作用及其提出的機械保護功能。這種機制保護與星形膠質細胞支持、引導和促進神經元生長的作用相吻合。此外,星形膠質細胞與血管密切相互作用,甚至調節血流和血管直徑,從而可能緩沖腦血管系統的機械負荷。該研究結果強調了機械力對發育和成體階段基本腦細胞特性的重要性,并深入了解了神經源性生態位中 NSCs 行為的復雜但未知的機制。
參考文獻:Abraham JA, Blaschke S, Tarazi S, Dreissen G, Vay SU, Schroeter M, Fink GR, Merkel R, Rueger MA, Hoffmann B. NSCs Under Strain-Unraveling the Mechanoprotective Role of Differentiating Astrocytes in a Cyclically Stretched Coculture With Differentiating Neurons. Front Cell Neurosci. 2021 Sep 24;15:706585. doi: 10.3389/fncel.2021.706585. PMID: 34630042; PMCID: PMC8497758.
原文鏈接:https://pubmed.ncbi.nlm.nih.gov/34630042/
小編旨在分享、學習、交流生物科學等領域的研究進展。如有侵權或引文不當請聯系小編修正。如有任何的想法以及建議,歡迎聯系小編。感謝各位的瀏覽以及關注!
微信搜索公眾號“Naturethink”,了解更多細胞體外仿生培養技術及應用。
點擊了解
細胞流體剪切力|共培養|壓力培養|牽張應變|血管培養|平行平板流動腔|儀器|上海泉眾機電科技有限公司Naturethink
Naturethink牽張力|拉伸力|細胞拉伸|細胞牽張|細胞牽張應變|牽張應變細胞培養儀