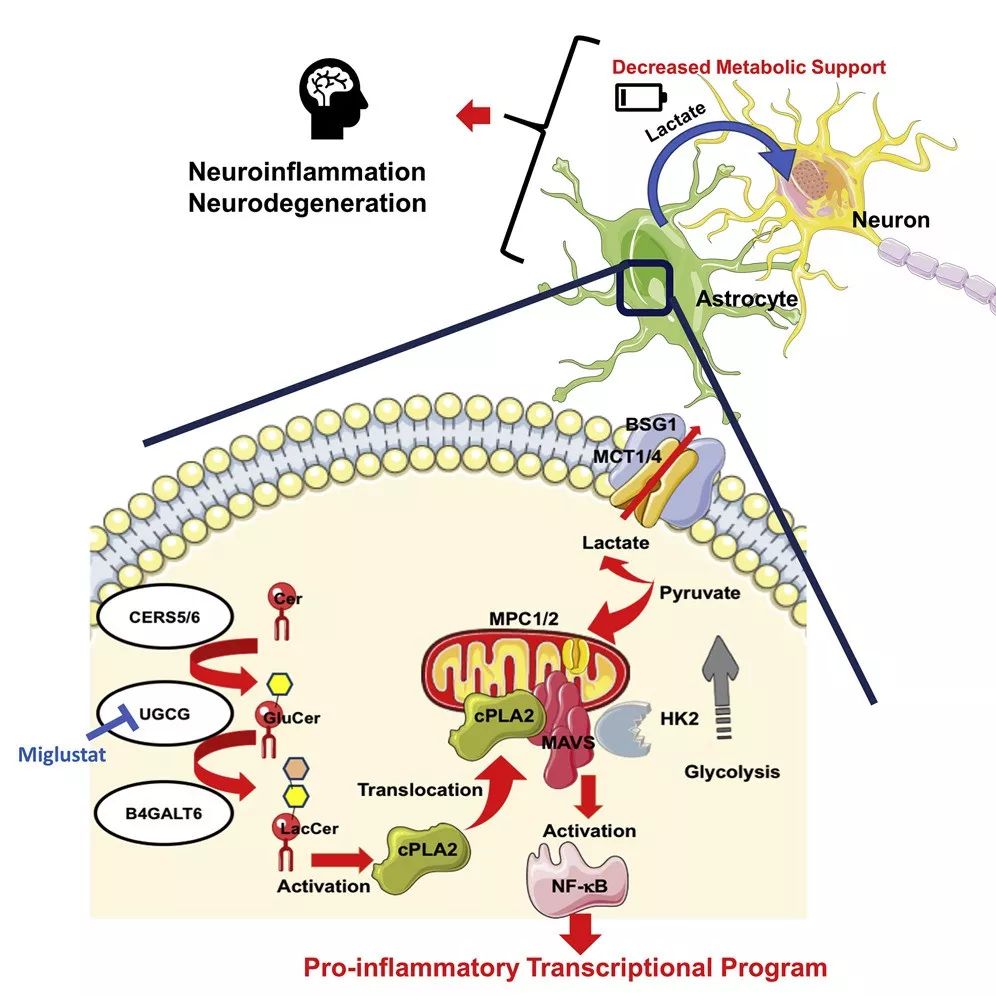
ЗКЦ¬ҙъЦxХ{ҝШРЗРОДzЩ|јҡ°ыФЪЦРҳРЙсҪӣПөҪyСЧ°YЦРөДЧчУГ
СРҫҝҲFк °l¬FЈ¬РЗРОДzЩ|јҡ°ыЦРөД cPLA2 өД C2 ҪYҳӢУтЕc MAVS ЦРөД CARD ҪYҳӢУтПа»ҘЧчУГЈ¬ФЪҢҚтһРФЧФЙнГвТЯРФДXј№ЛиСЧ (EAE) ТФј°қ“ФЪөД¶а°lРФУІ»Ҝ°Y (MS) ЦРЙПХ{ NF-ҰКB тҢК№өДЮDдӣЈ¬ҙЩЯMЦРҳРЙсҪӣПөҪy (CNS) өДСЧ°Y°lЙъЈ»cPLA2 ұ»ХРДјөҪ MAVSЈ¬ЖЖүДБЛ MAVS- јәМЗјӨГё 2 (HK2) йgөДПа»ҘЧчУГЈ¬ҪөөНБЛ HK өДГё»оТФј°…ўЕcЙсҪӣФӘҙъЦxөДИйЛбЛ®ЖҪЈ»Miglustat (Т»·NУЪЦОҜҹ Gaucher ІЎәН Niemann-Pick ІЎөДЛҺОп)Ј¬ДЬТЦЦЖРЗРОДzЩ|јҡ°ыөДЦВІЎ»оРФЈ¬ёДЙЖ EAEЎЈҝӮ¶шСФЦ®Ј¬Я@Р©°l¬F¶ЁБxБЛТ»·NДЬтҢ„УҙЩСЧРФРЗРОјҡ°ыөД»о„УөДРВөДГвТЯҙъЦxҷCЦЖЈ¬ёЕКцБЛ MAVS ФЪЦРҳРЙсҪӣПөҪyСЧ°YЦРөДРВЧчУГЈ¬һйЦОҜҹРФёЙоAМṩБЛәтЯx°РьcЎЈ
РЗРОДzЩ|јҡ°ыЦР LacCer ЙъОпәПіЙНҫҸҪҙЩЯM NOD EAE °lХ№
СРҫҝИЛҶTАыУГ·З·КЕЦМЗДтІЎ (NOD) РЎКуҪЁБўБЛ EAE ДЈРНЈ¬НЁЯ^ПакP»щТтұнЯ_әНЗГіэ·ЦОцЈ¬ҙ_¶ЁБЛРЗРОДzЩ|јҡ°ыЦРөДИйМЗЙсҪӣхЈ°· (LacCer) ЙъОпәПіЙНҫҸҪҙЩЯM NOD EAE өД°lХ№Ј¬ЧCГчБЛЗКЦ¬ҙъЦxтҢК№РЗРОДzЩ|јҡ°ы»о„УЈ¬ҙЩЯM CNS СЧ°Yј°ЙсҪӣНЛ»ҜЎЈ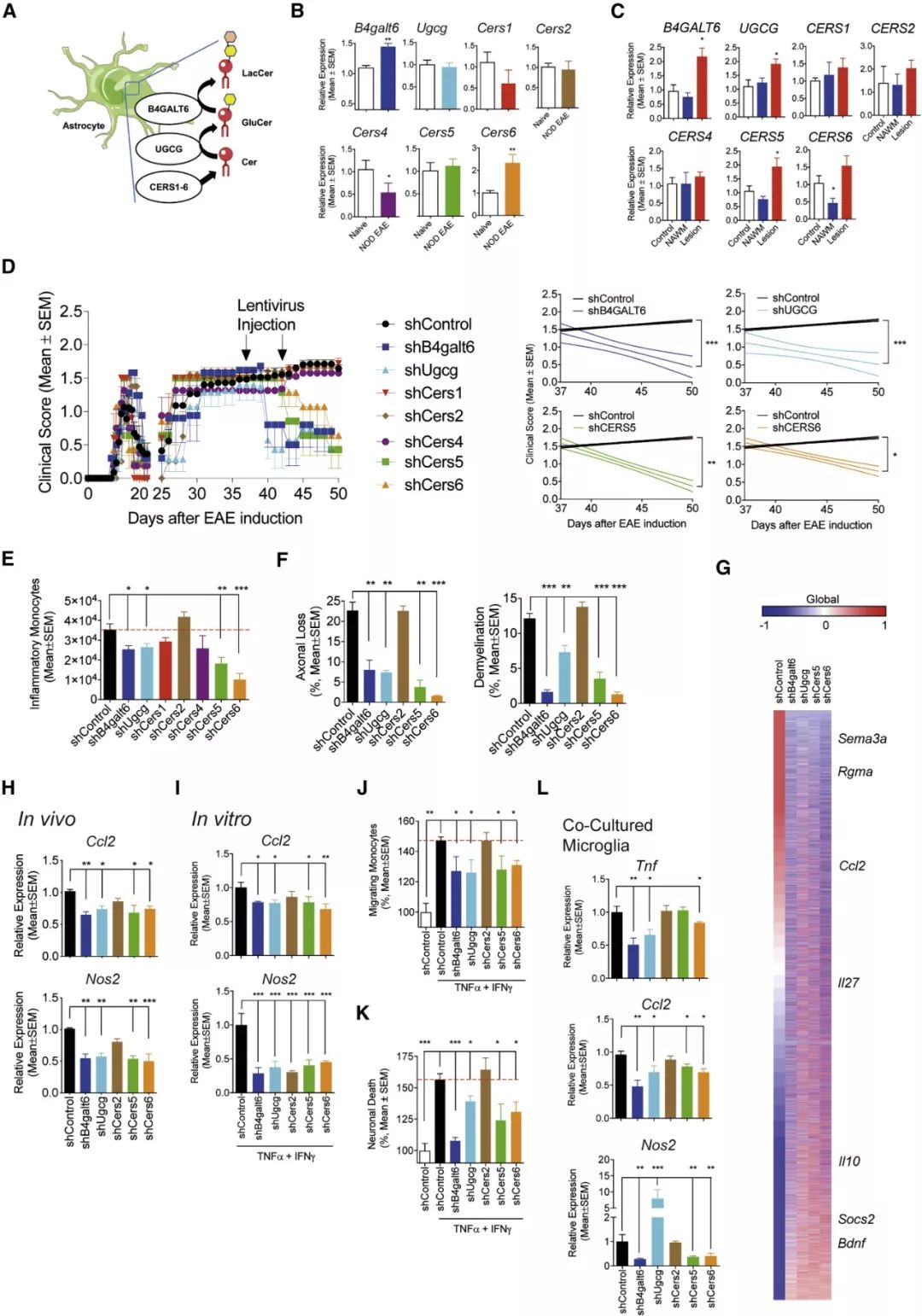
ҲD 1. РЗРОДzЩ|јҡ°ыЦРөД LacCer ЙъОпәПіЙНҫҸҪҙЩЯM NOD EAE ЯMХ№
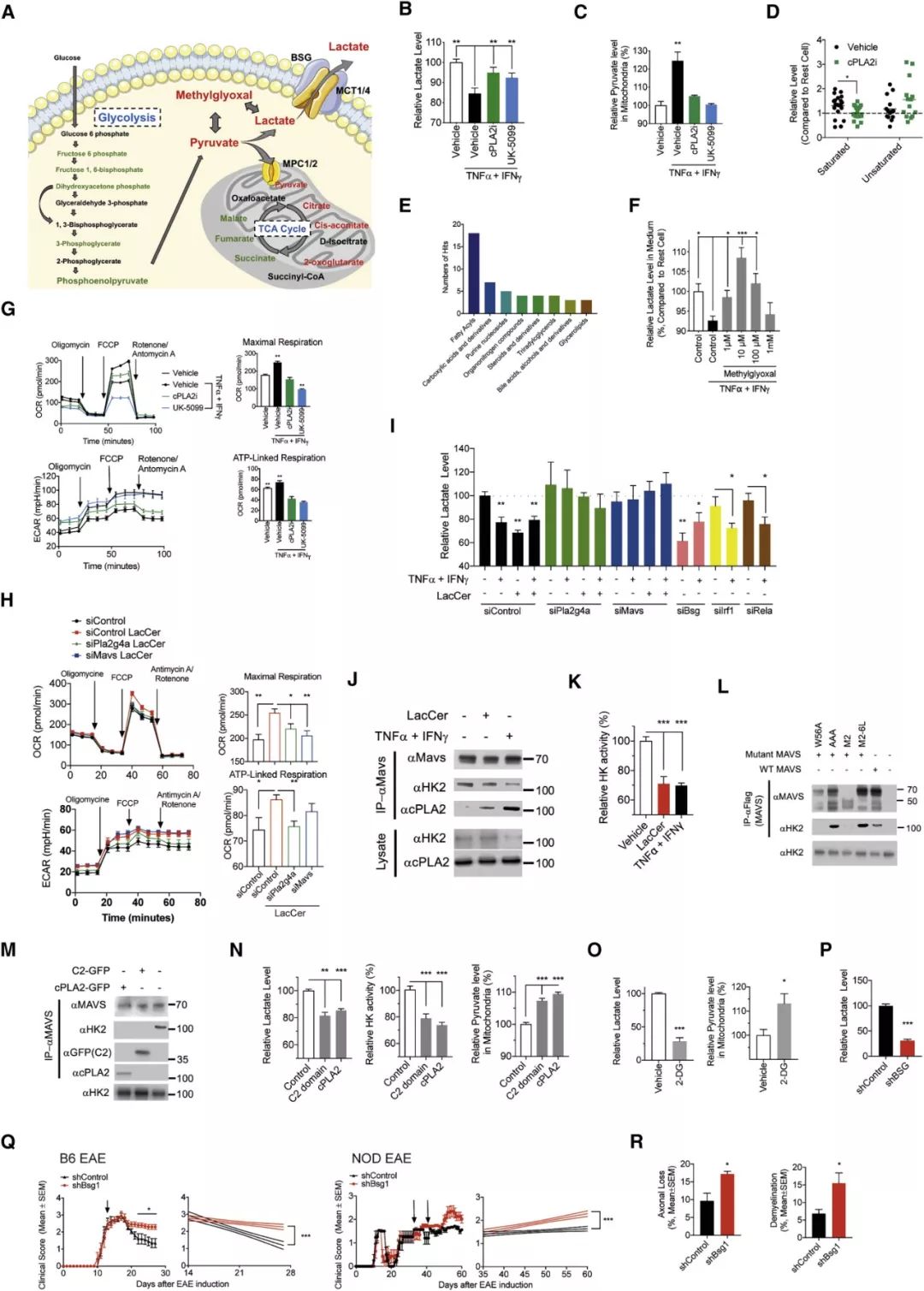
LacCer ХTҢ§өД cPLA2-MAVS РЕМ–ӮчҢ§тҢ„У NF-ҰКB ТАЩҮРФҙЩСЧіМРт
ТСЦӘ LacCer Еc cPLA2 Па»ҘЧчУГЈ¬НЁЯ^РЎКуәНРЗРОДzЩ|јҡ°ыЗГіэ PLA2G4A (ҫҺҙa cPLA2 өД»щТт) ҢҚтһЈ¬°l¬FБЛ LacCer НЁЯ^јӨ»о cPLA2 ЙПХ{РЗРОДzЩ|јҡ°ыЦР NF-ҰКB ТАЩҮРФҙЩСЧ°YЮDдӣіМРтЎЈ
НЁЯ^ПакP»щТтөДН»ЧғЕcЯ^ұнЯ_Ј¬CoIP Еc Western blot өИ·Ҫ·Ёҷzңy°l¬FЈ¬LacCer ХTҢ§ cPLA2 ЯMИлҫҖБЈуwІўЕc MAVS №І¶ЁО»Ј¬ cPLA2 өД C2 ҪYҳӢУтәН MAVS өД CARD ҪYҳӢУтҪйҢ§ cPLA2-MAVS Па»ҘЧчУГЈ¬јӨ»о MAVSЎЈТСЦӘ MAVS РЕМ–ҝЙТФҙЩЯM NF-ҰКB өДјӨ»оЈ¬ РЗРОДzЩ|јҡ°ы MAVS өДИұК§ТЦЦЖБЛ LacCer ХTҢ§өД NF-ҰКB әЛТЧО»ј°Жд°Р»щТтөДХРДјЈ¬ТФј° Nos2, Ccl2 әН Csf2 өДұнЯ_ЎЈЗГіэ Mavs ТЦЦЖБЛ NOD EAE ЯMХ№ІўңpЙЩ CNS ЦРҙЩСЧҶОәЛјҡ°ыөД·eАЫЈ¬ТФј°РЗРОјҡ°ыөДЦВІЎ»о„УПакP NF-ҰКB тҢ„УөДҙЩСЧ°Y»щТтөДұнЯ_ЎЈҪЎҝөҢҰХХәН MS ДXҳУұҫГвТЯҹЙ№в”ө“ю·ЦОцЯMТ»ІҪЧCГчЈ¬ЗКБЧЦ¬ҙъЦxНЁЯ^ cPLA2-MAVS РЕМ–ЭSјӨ»о NF-ҰКBЈ¬ҙЩЯMРЗРОДzЩ|јҡ°ыФЪ EAE әН MS ЦРөДЦВІЎ»о„УЎЈcPLA2-MAVS РЕМ–Х{ҝШРЗРОДzЩ|јҡ°ыРВкҗҙъЦx
СРҫҝИЛҶT·ЦОцБЛ LacCer-cPLA2 РЕМ–ҢҰРЗРОјҡ°ыҙъЦxөДУ°н‘ј° MAVS ФЪЖдЦРөДЧчУГ°l¬FЈ¬ҙЩСЧҙМјӨНЁЯ^ cPLA2-MAVS ХTҢ§ LacCer тҢ„УөДРЗ ојҡ°ыҙъЦxЧғ»ҜЈ¬ФцјУБЛұыНӘЛбөДҫҖБЈуwСх»ҜЈ¬ҸД¶шҪөөНИйЛбөД®aЙъәНбҢ·ЕЎЈҢҰСЧ°YтҢ„УөД cPLA2-MAVS РЕМ–ҢҰ MAVS Еc HK2 Па»ҘЧчУГөДУ°н‘СРҫҝ°l¬FЈ¬cPLA2 C2 ҪYҳӢУтҝЙДЬИЎҙъ HK2 Еc MAVS CARD ҪYҳӢУтПа»ҘЧчУГЈ¬cPLA2 өДЯ^ұнЯ_ЖЖүДБЛ HK2-MAVS Па»ҘЧчУГЈ¬Ң§ЦВ HK »оРФҪөөНЈ¬ИйЛб·ЦГЪңpЙЩЈ¬Н¬•rҫҖБЈуwұыНӘЛбЛ®ЖҪЙэёЯЎЈНЁЯ^ИйЛбЯ\Э”°ыНвПакPЮDЯ\ө°°Ч»щТтөДЗГіэЈ¬ҪТКҫБЛРЗРОДzЩ|јҡ°ыЦР cPLA2-MAVS ТэЖрөДИйЛббҢ·ЕңpЙЩҝЙДЬЕcЦРҳРЙсҪӣПөҪyІЎАнУРкPЎЈҫCЙПЛщКцЈ¬ФЪЦРҳРЙсҪӣПөҪyСЧ°YЯ^іМЦРЈ¬LacCer тҢ„УөДcPLA2-MAVS РЕМ–Х{ҝШРЗРОјҡ°ыөДҙъЦxј°ЖдЦ§іЦЙсҪӣФӘөДДЬБҰЎЈҲD 3. cPLA2-MAVS РЕМ–Х{№қРЗРОДzЩ|јҡ°ыҙъЦx
Miglustat ҫҸҪвВэРФ°lХ№өД EAE
УГ Miglustat (Miglustat hydrochloride ЩҸУЪ MedChemExpress) МҺАн NOD EAE РЎКу Ј¬іц¬FФЪ CNS ·eАЫЈ¬ТЦЦЖБЛ NOD EAE °lХ№Ј¬ұн¬FһйЕRҙІФu·ЦҪөөНЎўЭSН»ҒGК§ЎўГ“ЛиЗКәНҙЩСЧҶОәЛјҡ°ыөДДјјҜөҪ CNSЈ¬¶ш Mavs ЗГіэРЎКуЗйӣrӣ]УРөГөҪёДЙЖЈ¬ХfГч Miglustat өДЦОҜҹР§№ыЕc cPLA2-MAVS РЕМ–ПакPЎЈMiglustat ТЦЦЖБЛРЎКуәНИЛоҗРЗРОДzЩ|јҡ°ыЦР Pla2g4 әНҙЩСЧ»щТтөДұнЯ_Ј¬ҪөөНРЗРОДzЩ|јҡ°ыөДЙсҪӣ¶ҫРФЈ¬ТФј°ЛьӮғФЪЪ…»ҜҢҚтһЦРХРДјҶОәЛјҡ°ыәНјӨ»оРЎДzЩ|јҡ°ыөДДЬБҰЎЈ
ФӯОДжңҪУЈә Chao CC, et al. Metabolic Control of Astrocyte Pathogenic Activity via cPLA2-MAVS.Cell. 2019 Dec 12;179(7):1483-1498.e22.
ПакP®aЖ·Јә Miglustat hydrochloride КЗТ»·NЖПМСМЗЙсҪӣхЈ°·әПіЙГёТЦЦЖ„©Ј¬ҝЙЧчУГУЪ I РН Gaucher ІЎЎЈ
- PARPТЦЦЖ„©OlaparibөДЧчУГҷCАнј°ФЪҝЖСРЦРөД‘ӘУГ
- БЧЦ¬ҫЫТТ¶юҙјёКВ¶МЗ(DSPE-PEG2000-Mannose)өДҪYҳӢЎўМШРФЕc‘ӘУГ
- ТЯГзЧф„©QS-21өДЧчУГҷCАнј°ФЪТЯГзСРҫҝЦРөД‘ӘУГ
- ЙъОпЦёКҫ„©Чо¶МЕарB•rйgЈЁMITЈ©ңy¶ЁИ«РВ·Ҫ°ёҪйҪB
- ReadiLinҝ№уwҳЛУӣФҮ„©әРөДғһ„Эј°‘ӘУГҲцҫ°
- MST јјРgЦъБҰлyјғ»Ҝө°°ЧөДУHәНБҰ·ЦОц
- ТЦЦЖ„©BIIB021ФЪјҡ°ыҢҚтһәН„УОпҢҚтһөДИЬҪв·Ҫ°ё
- жңГ№УHәНЛШЕјВ“ОпөДғһ„Э
- ОчГАҪЬіЙ№Ұ…ўјУөЪ¶юК®ЛДҢГЦРҮшЙъОпЦЖЖ·ҙу•ю
- 2025AACRДк•юҲAқMВдД»Ј¬MCE”yФҮ„©®aЖ·ББПаЦҘјУёз
- ОчГАҪЬіЙ№Ұ…ўјУөЪК®ҢГЙъОпЦЖЛҺ·Җ¶ЁРФХ“үҜ
- Н¶ёеУР¶Y-2025 MCEЦРҮшЙъГьҝЖҢWСРҫҝҙЩЯMӘ„ХэКҪҶў„У
- °¬ӮҘНШ&°ІНШЛј•юЧhСыХҲЈәјҜІЙ•rҙъөДҸНлsЦЖ„©РВ·ҪПт
- й_ҢWјҫЈ¬ҝЖСРёЈАыөҪ!ұҫЙъЙъОпМбИЎФҮ„©әРПЮ•rМШ»Э
- Оч°І°ЩОһЙъОпАТ°·ИҫБППЮ•rҙЩдNЈ¬ЩҸЩIјҙГвЩMЛНлҠУ°Жұ
- ГАөВВ•НЖіцНЁЯ^LC-MS/MS”UҙуРВЙъғәәYІйөДҷzңyФҮ„©