默克BioReliance®檢測服務應邀參加PMIO 2020

默克BioReliance®檢測服務應邀參加2020第三屆中國精準醫學與腫瘤免疫治療峰會
繼抗體免疫療法的高速發展后,以CAR-T產品為代表的體內/體外基因治療策略已經成為進5年來藥物開發的新興行業。據初步統計,全球已經有超過1000個細胞基因治療的臨床實驗。這預示著新型的基因治療療法全面到來。然而在新興產業進入全面產業化布局的過程中,仍然存在著諸多有待解決或提高的方面。其中,生產工藝中原材料,過程產品和終產品的合規化檢測技術發展和靈活高效的測試需求是商業化放大中集中關注的熱點。如何以高效,準確,合規的檢測技術方式確保藥物的安全有效,一直是默克BioReliance®檢測服務持續努力的方向。
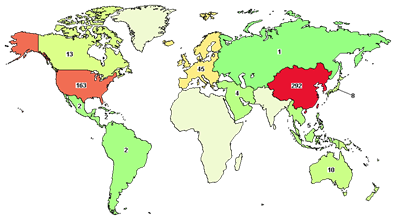
全球CAR-T 臨床實驗統計 (2020/5/13) Clinicaltrials.org
作為一家有著70多年歷史的檢測服務機構,默克BioReliance®檢測服務始終以法規更新作為服務導向,具備符合EMA,FDA,ICH等不同法規要求的專業服務體系,向全球客戶提供了包括生物安全性檢測,細胞株建庫鑒定,病毒清除驗證,產品批放行測試,生物分析檢測,產品表征測試等超過1000種經驗證的檢測服務。已為全球超過1000家生物制藥和基因治療客戶提供過高質量的檢測技術服務。
為切合當下“整合產業科技,助力制藥創新“的主題,默克BioReliance®檢測服務應邀參加2020第三屆中國精準醫學與腫瘤免疫治療峰會,和600多位與會嘉賓共話基因治療產品質量檢測考量的主題。會議中,王鑫博士代表默克BioReliance®檢測服務向與會嘉賓介紹了基于基因治療生產工藝所衍生的產品質量風險點以及合規化的檢測技術方案。特別針對在CAR-T細胞治療類產品中關于慢病毒可復制性(RCL)檢測方面進行了重點闡述,作為中國境內少數能提供RCL測試的服務方,默克BioReliance®檢測已經為多家中國客戶提供過相關服務。

默克BioReliance®檢測服務應邀參加2020第三屆中國精準醫學與腫瘤免疫治療峰會
新型的基因治療類產品,通常依托核酸,病毒載體,細胞載體等具有生物活性的介質發揮其治療作用。與傳統意義上的藥物相比,在安全性和質量放行方面有更為嚴格的要求。因此,FDA于2020年出正式出版了關于基因治療類產品的CMC指導,我國2020版藥典中也增加了人用基因治療類產品總論。為積極響應全球不同法規體系的更新,默克BioReliance®檢測服務以科學與法規的專業知識,全面的技術覆蓋(理化,分子,細胞,動物等)為客戶提供包括病毒庫/菌種庫/細胞庫建庫,細胞系鑒定,質粒/病毒過程產品檢測,終產品批釋放檢測以及產品表征檢測等合規化服務。并依托全球化的業務集群為產品,特別是生物治療(抗體,基因治療)產品的多地檢測申報提供靈活便捷渠道。
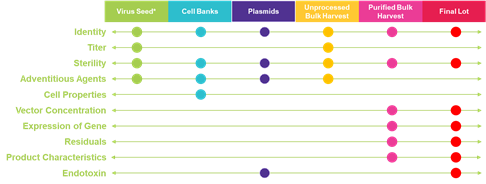
默克BioReliance®檢測服務基因治療檢測服務簡介
在此,我們誠摯期待與您攜手,以專業的服務態度,共同加速新型基因治療類產品的商業化進程。詳細業務咨詢請掃描如下二維碼。

默克BioReliance®檢測服務基因治療檢測服務咨詢
- 艾貝泰邀您參加上海ISPE 2025國際制藥工程大會
- BIOHK2025年第4屆香港國際生物科技論壇暨展覽通知
- Rocker實驗室設備即將亮相2025 臺北食品&生技展
- 易科泰攜前沿生態技術產品精彩亮相智慧農業論壇
- 2025第九屆亞太生物醫藥合作峰會通知
- 慧榮和成功參展毒理學會中藥與天然藥物毒理專委會
- 安捷倫科技在 ACCSI 2025 展示本地化戰略成果
- 慧榮和參加第九屆空氣生物學與生物凈化防護研討會
- 2025第二屆合成生物制造創新發展大會議程首發
- 27國技術集結上海,2025Medtec醫療器械展邀您參觀
- PMEC 2025實驗室創新與發展論壇報名已開啟
- 10x邀您參加單細胞與空間多組學前沿峰會-北京站
- 2026(第八屆)中國國際生物醫藥大會暨展覽會通知
- 諾澤攜超微氣流粉碎機等參展2025春季藥機展CIPM
- 武漢谷豐光電精彩亮相2025農業生物表型組學研討會
- 10x Genomics技術方案更新(4月),新手冊邀您領取
- 10x邀您參加單細胞與空間多組學前沿峰會-北京站
- 真邁FASTASeq 300 Dx獲批NMPA三類醫療器械注冊證
- 第五屆多組學科研與臨床應用大會五一福利大放送
- ATMP 2025第九屆先進療法創新峰會通知
- 安捷倫在AACR 2025展示開創性解決方案與合作成果
- 10x Genomics技術方案更新(3月),新手冊邀您下載
- 安捷倫胃腺癌等伴隨診斷檢測產品獲得歐盟IVDR認證
- 森西賽智亮相中國細胞生物學學會2025年全國大會
- 森西賽智科技受邀亮相第七屆病毒腫瘤學學術會議
- 怡美通德誠邀您參加CCTB 2025腫瘤標志物學術大會
- 中山大學王鵬教授榮獲安捷倫ACT-UR研究基金支持
- 森西賽智聯合Vizgen在兩場大會正式推出MERFISH2.0
- 怡美通德邀您參加第三屆國際單細胞及空間組學大會
- 10x Genomics技術方案更新(2月),新手冊等您獲取
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com






